Contato:Errol Zhou (Senhor.)
Telefone: mais 86-551-65523315
Celular/WhatsApp: mais 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Adicionar:1002, Huanmao Edifício, Nº 105, Mengcheng Estrada, Hefei Cidade, 230061, China
A Spero Therapeutics está comprometida com o desenvolvimento e comercialização de medicamentos para o tratamento de infecções bacterianas multirresistentes (MDR) e doenças raras. Recentemente, a empresa anunciou que apresentou um Pedido de Novo Medicamento (NDA) para comprimidos de antibiótico tebipenem HBr oral (anteriormente conhecido como SPR994) para a Food and Drug Administration (FDA) dos EUA: para o tratamento de infecções complexas do trato urinário causadas por suscetíveis microrganismos (CUTI, incluindo pielonefrite). Se aprovado, o tebipenem HBr se tornará o único antibiótico carbapenêmico oral que pode ser usado para tratar UTIc, o que mudará a prática clínica.
A submissão do NDA é baseada nos dados positivos do estudo de Fase 3 ADAPT-PO comunicados anteriormente. Os resultados mostraram que o estudo atingiu o objetivo primário: no tratamento de cUTI e pielonefrite aguda (AP), a eficácia do tebipenem HBr oral foi estatisticamente não inferior à do ertapeném (ertapenem) intravenoso (IV).
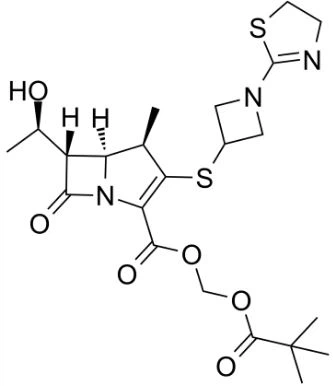
A estrutura química do Tippenem Pivoxil (fonte da imagem: medchemexpress.com)
Tebipenem HBr é uma nova preparação oral de tebipenem pivoxil. O éster tippenem é um antibiótico carbapenem β-lactâmico. É comercializado no Japão pela Meiji Pharmaceutical Co., Ltd. (Meiji) desde 2009 (nome comercial Orapenem) para o tratamento de pneumonia limitada, otite média e infecções pediátricas de sinusite. Os antibióticos carbapenêmicos são uma subclasse importante de antibióticos porque são seguros e eficazes no tratamento de infecções por bactérias Gram-negativas resistentes.
tebipenem HBr foi desenvolvido para tratar UTIc e pielonefrite aguda (PA). Anteriormente, o FDA dos EUA concedeu ao tebipenem HBr o produto qualificado para doenças infecciosas (QIDP) e qualificação de via rápida (FTD) para o tratamento de cUTI e AP. Se aprovado, o tebipenem HBr se tornará o primeiro antibiótico carbapenêmico oral a ser comercializado nos Estados Unidos.
Ankit Mahadevia, MD, CEO da Spero Therapeutics, disse:" Com a apresentação do NDA, demos um passo importante em direção ao nosso objetivo de fornecer tratamentos orais para a maioria dos pacientes cUTI. Este tratamento oral pode substituir a terapia intravenosa (IV) de uso prolongado. Se aprovado, acreditamos que o tebipenem HBr pode ajudar significativamente os pacientes e evitar a redução na utilização de recursos médicos que podem ser causados pela injeção intravenosa. Esperamos trabalhar com o FDA durante o processo de revisão do NDA e fornecer tebipenem HBr em 2022 Preparação para a listagem esperada em seis meses."

Dados do estudo clínico ADAPT-PO
ADAPT-PO é um ensaio clínico de fase 3 controlado por placebo, randomizado, conduzido em pacientes adultos hospitalizados com cUTI ou AP para avaliar a eficácia e segurança do tebipenem HBr. Neste ensaio, os pacientes foram divididos aleatoriamente em grupos na proporção de 1: 1. Um grupo recebeu tebipenem HBr (600 mg por via oral, uma vez a cada 8 horas), e o outro grupo recebeu ertapenem (1 g, infusão intravenosa, uma vez a cada 24 horas). ), um total de 7 a 10 dias de tratamento. Pacientes com bacteremia recebem até 14 dias de tratamento. O endpoint primário do estudo é: a taxa de resposta geral (ORR) no momento da visita do teste de cura (TOC) (dia 19 ± 2) na população micro-ITT, definida como cura clínica + patogênica os microorganismos erradicam.
Os resultados mostraram que o estudo atingiu o desfecho primário: na visita de TOC da população micro-ITT, o tebipenem HBr oral não foi inferior ao ertapenem IV na ORR. Os dados específicos são: a ORR do grupo de tratamento com tebipenem HBr é 58,8% (264/449), e a ORR do grupo ertapenem é 61,6% (258/419) (diferença de tratamento: -3,3%; IC de 95%: - 9,7, 3,2; valor de corte de não inferioridade [NI] é -12,5%). A ORR foi consistente em todos os subgrupos principais (incluindo idade, diagnóstico inicial e presença de bacteremia). Para os patógenos mais comuns do trato urinário, a resposta de cada grupo de tratamento a cada microorganismo patogênico foi balanceada.
Além disso, o estudo também alcançou desfechos secundários importantes: a taxa de cura clínica em visitas de TOC em ambos os grupos foi maior (& gt; 93%), 93,1% no grupo tebipenem HBr oral e 93,6% no grupo ertapenem IV . Neste estudo, o tebipenem HBr foi bem tolerado e seu perfil de segurança foi semelhante ao ertapenem IV.